Darmkrebs
Dickdarmkrebs
Ein Dickdarmkrebs wird in der Regel im Gegensatz zum Enddarmkrebs nach Diagnosestellung und Klärung der Operationsfähigkeit durch eine Operation entfernt. Hierbei sind folgende Operationsziele zu erreichen:
1. Muss der Tumor selbst durch den Eingriff vollständig beseitigt sein, was sowohl bei Patient*innen sinnvoll ist, bei denen eine gute Heilungschance besteht (dies ist beim Dickdarmkrebs die Regel) als auch bei Patient*innen, bei denen eine dauerhafte Heilung wegen zu großer Tumorausdehnung (dies ist bei Diagnosestellung seltener der Fall) nicht mehr möglich ist und
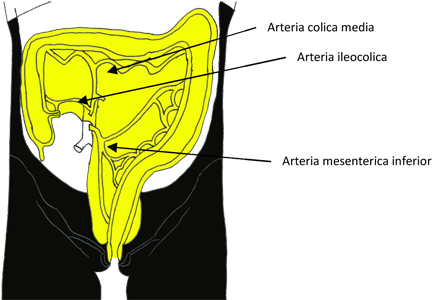
2. Wird das zum Tumor gehörende Lymphabflussgebiet (Abb. 1) entfernt, damit hier vorhandene tumornahe Lymphknotenabsiedlungen entfernt werden. Hierbei orientiert man sich an den darmversorgenden Arterien, da die nicht sichtbaren Lymphgefäße hierzu parallel verlaufen. Bei der seltenen Infiltration von Nachbarorganen (Blase, Dünndarm etc.) kann durch Mitnahme infiltrierter Strukturen häufig noch eine vollständige Entfernung des Tumors erreicht werden.
Da die unterschiedlichen Anteile des Dickdarms eine unterschiedliche Gefäßversorgung haben, richtet sich die Art und Ausdehnung der Operation (Resektionsverfahren) wesentlich danach, wo der Tumor im Dickdarm vorliegt.
Abb. 1
Operation
Standardresektionsverfahren sind: Hemikolektomie rechts: (bei Tumor im Caecum oder Colon ascendens): Resektion von Caecum, Colon ascendes, Arteria und Vena Ileocolica und colica dextra mit zugehörigem Lymphabfußgebiet. Transversumresektion: (bei Tumor im Colon transversum) Resektion von Colon transversum, Arteria und Vena colica media mit Lymphabflussgebieten sowie dem Omentum majus (sogenanntes großes Netz). Hemikolektomie links: (Tumor im Colon descendens) Resektion des Sigma, Colon descendens, linke Flexur, Arteria und Vena mesenterica inferior. Sigmaresektion: (Tumor im Colon sigmoideum) Resektion des Colon sigmoideum, distales Colon descendens, Arteria und Vena mesenterica inferior.
Wiederherstellung der Darmpassage
Nach der Entfernung des tumorbefallenen Darmanteils sowie seines Lymphabflussgebietes muss die Passage wiederhergestellt werden: Die Darmkontinuität wird durch eine genähte End-zu-End-Verbindung (Anastomose) wiederhergestellt. Für eine ungestörte Heilung der Anastomose ist die gute Durchblutung der Darmenden, die spannungsfreie Anlage und die wasserdichte, jedoch die Durchblutung nicht kompromittierende Naht entscheidend.
Da die Versorgung des Darms mit Blut in der Situation des Darmverschlusses (Ileus) gestört ist, ist die Gefahr einer gestörten Anastomosenheilung in dieser Situation erhöht. Aus diesem Grund kann bei Vorliegen von Notfallsituationen wie zum Beispiel beim Darmverschluss oder beim Darmdurchbruch notwendig sein, die Nahtverbindung erst verzögert, also zum Beispiel drei Monate später nach vorübergehender Anlage eines künstlichen Darmausgangs anzulegen.
Absiedlungen (Metastastasen)
Prinzipiell sind zwei Wege denkbar, auf denen ein Dickdarmkrebs metastasieren kann: über die Lymphbahnen (sogenannte lymphogene Metastasierung) und über das Blut in Leber und Lunge (sogenannte hämatogene Metastasierung). Während bei lymphogener Metastasierung häufig durch die Operation und eine zusätzliche Chemotherapie eine Heilung erreicht werden kann, ist dies bei einer hämatogenen Metastasierung in Leber und Lunge nur bei einem kleinen Teil der Patient*innen möglich, wenn eine vollständige Entfernung der Metastasen durch Operation erreicht werden kann. Sollte das Tumorleiden hierzu zu fortgeschritten sein, so kann oft noch eine wesentliche Lebensverlängerung durch eine Chemotherapie auch bei diesen Patient*innen erreicht werden.
Operationsrisiken
- gestörte Heilung der zusammengefügten Darmenden (bei etwa 1 bis 3 Prozent der Operationen) mit der Gefahr der Bauchfellentzündung (Anastomoseninsuffizienz mit Peritonitis und Sepsis), was eine erneute Operation, ggf. dann mit Anlage eines vorübergehenden künstlichen Darmausgangs zur Folge haben kann
- Nachblutung, Bluttransfusion (AIDS, Virushepatitis)
- Wundinfekt
- Verletzung von Nachbarstrukturen wie zum Beispiel Milz oder Harnleiter
Zugang zum Operationsgebiet – „Laparoskopisch oder offen“
Während bis vor wenigen Jahren die Operation bei Dickdarmkrebs immer über einen großen Bauchschnitt („offene Operation“) vorgenommen werden musste, ist heute nachgewiesen, dass auch bei der Tumorerkrankung des Dickdarmes in geübter Hand die minimalinvasive = laparoskopische Operation (sogenannte Schlüssellochchirurgie) gleichwertig der „offenen Operation“ ist. Vorteile des minimalinvasiven Zugangs sind vor allem für die Zeit unmittelbar nach der Operation nachgewiesen (kürzerer Krankenhausaufenthalt, geringerer Blutverlust, früheres Einsetzen der normalen Darmfunktion etc.). Weit wichtiger als diese Vorteile ist die Erfahrung des Operateurs und des behandelnden Krankenhauses mit der Erkrankung (z. B. erkennbar an der Anzahl behandelter Dickdarmtumorpatient*innen). Ein weiterer bekannter Vorteil dieser Technik liegt in dem deutlich selteneren Auftreten von Narbenbrüchen nach minimalinvasiver Operation im Vergleich zu der „offenen Operation“. Aus diesen Gründen ist die laparoskopische Technik in der Mindener Klinik das Standardverfahren in der Behandlung des Dickdarmkrebses.
Wie ist der praktische Ablauf vor, während und nach der Operation (Perioperativer Ablauf)?
Vor der Operation muss in der Regel schon vor einer Aufnahme in dem Krankenhaus die Diagnose durch eine Dickdarmspiegelung gestellt werden, ein weiterer Dickdarmtumor ausgeschlossen werden und durch Sonographie oder Computertomographie sowie eine Röntgenaufnahme der Lunge das Vorliegen von Absiedlungen in Leber und Lunge überprüft werden. Des Weiteren muss die Operationsfähigkeit geprüft werden. Anschließend kann dann der Operationstermin festgelegt werden. In der modernen Dickdarmchirurgie wird das so genannte „Fast Track Konzept“ angewandt. Dies bedeutet, dass keine Darmspülung vor der Operation notwendig ist, kurz vor der Operation ein „Rückenmarkskatheter“ gelegt wird und unmittelbar nach der Operation wieder mit der Aufnahme von Nahrung begonnen und der*die Patient*in frühzeitig aus dem Bett mobilisiert wird. Dies setzt eine optimale Schmerzbehandlung voraus. Auf Drainagen und „Schläuche“ wird in der Regel verzichtet. Bei der Mehrzahl der Patient*innen führt dieses Vorgehen zu einer wesentlich schnelleren Genesung, als eine traditionelle Nachbehandlung.
Enddarmkrebs
Die aktuelle Behandlung des Enddarmkrebses unterscheidet sich in mehrfacher Hinsicht von der des Dickdarmkrebses. Alle Patient*innen mit einem Enddarmkrebs sollten in einer interdisziplinären Tumorkonferenz vor Therapiebeginn besprochen werden, in der dann gemeinsam das optimale Therapiekonzept für den*die Patient*in festgelegt wird, um es anschließend mit dem Patienten zu besprechen.
Bei der Mehrzahl der Patient*innen liegt zum Zeitpunkt der Diagnose ein Tumorstadium vor, bei dem zunächst über mehrere Wochen eine kombinierte Strahlen- und Chemotherapie vorgenommen wird, die häufig zu einem wesentlichen Rückgang der Tumorgröße führt. Anschließend wird dann eine Operation mit Entfernung des Tumors sowie seines Lymphabflussgebietes vorgenommen. Die Weiterentwicklung der Operationstechnik hat im letzten Jahrzehnt zu einem der entscheidenden Fortschritte in der Behandlung des Enddarmkrebses geführt. Chirurgen, die in exakter Form die so genannte TME-Technik (Präparation in der so genannten mesorektalen Hüllfaszie nach Jonnesco) anwenden (Abb. 2), sehen bei ihren Patienten in weniger als 10 Prozent ein Wiederauftreten des Tumors an ihrem Entstehungsort, während diese Zahl früher im Extremfall bei 30-40% lag. Damit stellt gerade beim Enddarmkrebs die Expertise des Operateurs einen der entscheidenden Prognosefaktoren für einen Patienten mit einem Enddarmkrebs dar.
Die Operation kann bei entsprechender Erfahrung und unter bestimmten Voraussetzungen minimalinvasiv (Schlüssellochtechnik) oder aber „offen“ vorgenommen werden.
Abb. 2

Bei wenigen Patient*innen liegt zum Zeitpunkt der Diagnose ein so frühes Tumorstadium vor, dass der Enddarm nicht entfernt werden muss, sondern der Tumor durch den Darmausgang aus der Darmwand ausgeschnitten werden kann, was einen deutlich kleineren operativen Eingriff darstellt. Diese Situation stellt jedoch eine seltene Ausnahme dar.
Auf der anderen Seite gibt es wenige Patient*innen, bei denen zum Zeitpunkt der Operation ein Tumor vorliegt, der in ein Nachbarorgan eingewachsen ist. Hier ist in der Regel eine Strahlen- und Chemotherapie mit anschließender Entfernung des Enddarms und des benachbarten Organs erforderlich. Ein solcher Eingriff sollte nur in einer Klinik vorgenommen werden, in denen alle notwendigen Fachbereiche vorgehalten werden.
Damit hängen die Entscheidungen, welche Behandlungsschritte beim Enddarmkrebs eingeschlagen werden, von zwei Untersuchungen ab, die die Lokalisation und das Ausmaß des Tumors an seinem Entstehungsort vor Behandlungsbeginn bestimmen: die Rektoskopie, die den Abstand vom Darmausgang ausmisst (Abb. 3a), und die Endosonographie (Abb. 3b), die die Eindringtiefe des Tumors am Entstehungsort untersucht. Manchmal muss die Endosonographie durch eine so genannte Magnetresonanztomographie (MRT) ergänzt werden. Weitere notwendige Untersuchungen stellen fest, ob Leber und Lunge frei von Absiedlungen (Metastasen) sind.
Abb. 3
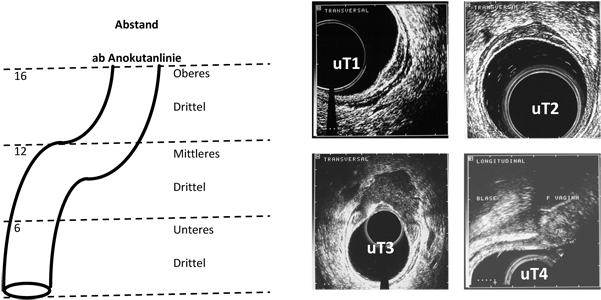
Abb. links: Bestimmung des Tumorabstandes vom Darmausgang durch starre Rektoskopie
Abb. rechts: Bestimmung der Eindringtiefe des Tumors in die Enddarmwand durch Endosonographie
Künstlicher Darmausgang
Für den*die Patient*in stellt sich bei sehr nah am Schließmuskel gelegenen Tumoren die Frage, ob der Schließmuskel bei der Operation erhalten werden kann und damit ein dauerhafter künstlicher Darmausgang vermieden werden kann. Hierzu muss bei einem Teil der Patienten ein vorübergehender Darmausgang (protektives Stoma) angelegt werden, um die Nahtverbindung (Anastomose) zu schützen. Bei diesen Patienten kann der künstliche Darmausgang durch einen kleinen operativen Eingriff wieder zurück verlagert werden. Die Entscheidung, ob der Schließmuskel erhalten werden kann, hängt davon ab, ob bei der Messung mit einem starren Rektoskop (Enddarmspiegelung) der Tumor mehr als 4 bis 5 cm vom Darmausgang (Anokutanlinie) entfernt ist. Tumoren, die mit ihrem Unterrand unterhalb dieser Grenze liegen, erfordern eine Amputation des Schließmuskels.
Operationsrisiken
- gestörte Heilung der zusammengefügten Darmenden (bei ca. 7 bis 15 Prozent der Operationen) mit der Gefahr der Bauchfellentzündung (Anastomoseninsuffizienz mit Peritonitis und Sepsis), was eine erneute Operation, ggf. dann mit Anlage eines vorübergehenden künstlichen Darmausgangs zur Folge haben kann
- Nachblutung, Bluttransfusion (AIDS, Virushepatitis)
- Wundinfekt
- Verletzung von Nachbarstrukturen wie zum Beispiel Milz oder Harnleiter
- Potenzstörungen, Harnentleerungsstörungen
Für alle Operationen beim Enddarmkrebs gilt, dass es sich um sehr anspruchsvolle Eingriffe handelt, die neben einer guten Expertise der Kooperationspartner in der Strahlentherapie und der Onkologie vor allem auch eine große Erfahrung des Operateurs in den modernen Operationstechniken beim Enddarmkrebs erfordern.
Nachsorge
Nachsorgeverantwortliche*r Arzt oder Ärztin
Während der Akutbehandlung Ihrer Krebserkrankung (Operation, eventuell Chemo- und Strahlentherapie) legen Sie nach Beratung mit Ihren Ärztinnen und Ärzten fest, welcher Arzt oder welche Ärztin die Tumornachsorge bei Ihnen koordinieren soll. Idealerweise legen Sie diesen schon nach Diagnosestellung gemeinsam mit Ihrem Hausarzt oder Ihrer Hausärztin fest. Die Tumornachsorge kann entweder von Ihrem Hausarzt oder Ihrer Hausärztin selbst oder einem durch ihn in Absprache mit Ihnen festgelegten Arzt bzw. Ärztin erfolgen. Spätestens nach der Operation wird im Entlassungsbrief der durch Sie benannte Nachsorgeverantwortliche Arzt bzw. Ärztin aufgeführt sowie ein für Sie nach allgemeinen Leitlinien festgelegtes Nachsorgeprogramm empfohlen.
Ernährungstipps
Rezeptbroschüren zur Darmkrebsaktion
Im Rahmen der Darmkrebsaktion der Deutschen Krebsgesellschaft e.V. sind Rezeptsbroschüren in Zusammenarbeit mit der Ernährungsberaterin Elisabeth Gutzmann und vielen Sterneköchen erschienen, darunter unter anderem Thomas Kammeier aus Berlin, Patrick Coudert aus München, Detlef Schlegel aus Leipzig, Claudio Urro aus Stuttgart sowie den Spitzenköchen Sten Fischer aus Weimar, Dieter Grubert aus Hannover, Hermann Krasenbrink aus Kassel und Claus Alboth aus Erfurt. Darüber hinaus ist eine Broschüre zu „Leckeren Brotaufstrichen“ erhältlich.
Patientinnen und Patienten mit einer Krebserkrankung müssen sich häufig zum Essen überwinden, weil der Appetit und die Verträglichkeit durch die Nebenwirkungen der Therapie beeinträchtigt sein können. Dabei sind Energie und eine ausreichende Nährstoffzufuhr ein wichtiger Aspekt und grundlegende Voraussetzung für die Behandlung. Die Broschüren bieten Anregungen für die gesunde und köstliche Küche sowie gut verträgliche Produkte. Die Rezepte der Sterneköche beinhalten leicht verdauliche, nährstoffreiche und vollwertige Menüs für Darmkrebspatient*innen und Ernährungstipps zur Prävention. Die vorgestellten Drei-Gänge-Menüs, die einfach nachgekocht werden können, bestehen vorwiegend aus frischen und regionalen Zutaten.
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Claus Alboth
Entstanden im Rahmen der Darmkrebsaktion 2008 der DKG
Erfurth, 7.6.2008
<link fileadmin user_upload johannes_wesling_klinikum_minden downloads rezeptbroschuere_alboth.pdf _blank download herunterladen der datei>Rezepte von Sternekoch Claus Alboth
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Dieter Grubert
Entstanden im Rahmen der Darmkrebsaktion 2008 der DKG
Hannover, 24.5.2008
<link fileadmin user_upload johannes_wesling_klinikum_minden downloads rezeptbroschuere_grubert.pdf _blank download herunterladen der datei>Rezepte von Sternekoch Dieter Grubert
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Hermann Krasenbrink
Entstanden im Rahmen der Darmkrebsaktion 2008 der DKG
Kassel, 17.5.2008
<link fileadmin user_upload johannes_wesling_klinikum_minden downloads rezeptbroschuere_krasenbrink.pdf _blank download herunterladen der datei>Rezepte von Sternekoch Hermann Krasenbrink
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Sten Fischer
Entstanden im Rahmen der Darmkrebsaktion 2008 der DKG
Suhl, 15.3.2008
<link fileadmin user_upload johannes_wesling_klinikum_minden downloads rezeptbroschuere_fischer.pdf _blank download herunterladen der datei>Rezepte von Sternekoch Sten Fischer
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Claudio Urru
Entstanden im Rahmen der Darmkrebsaktion 2008 der DKG
Stuttgart, 8.3.2008
<link fileadmin user_upload johannes_wesling_klinikum_minden downloads rezeptbroschuere_urru.pdf _blank download herunterladen der datei>Rezepte von Sternekoch Claudio Urru
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Detlev Schlegel
Auflage, 2007
Entstanden im Rahmen der Darmkrebsaktion 2008 der DKG
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Patrick Coudert
Entstanden im Rahmen der Darmkrebsaktion 2007 der DKG
Bon Appétit - Ernährungstipps für Darmkrebspatienten und Interessierte
Rezepte von Sternekoch Thomas Kammeier
Entstanden im Rahmen der Darmkrebsaktion 2007 der DKG
<link fileadmin user_upload johannes_wesling_klinikum_minden downloads rezeptbroschuere_kammeier.pdf _blank download herunterladen der datei>Rezepte von Sternekoch Thomas Kammeier